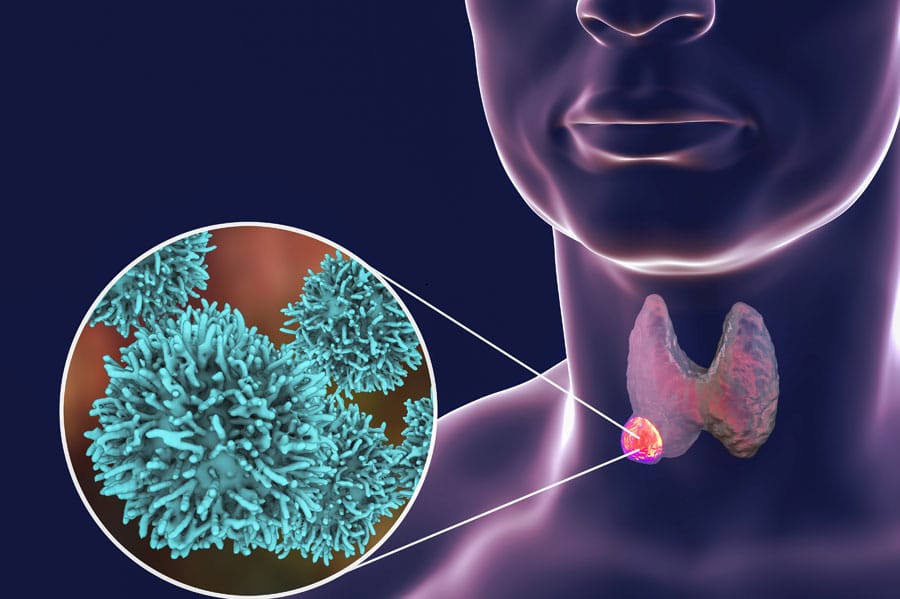
Depuis quelques années, la prise en charge du cancer de la thyroïde a été améliorée par de nouvelles recommandations. Ainsi, aujourd’hui, un parcours de soins personnalisés est proposé aux patients. Prise en compte des particularités de chacun, interventions moins invasives et plus confortables, adaptation des protocoles… tour d’horizon des nouvelles recommandations pour la prise en charge du cancer de la thyroïde.
Prise en charge du cancer de la thyroïde : qu’est-ce qui a changé ?
Les nouvelles lignes directrices concernant la prise en charge du cancer différencié de la thyroïde reflètent les grandes avancées cliniques et scientifiques qui ont eu lieu dans ce domaine et qui ont permis d’améliorer le quotidien de nombreux malades.
En Europe, c’est l’European Thyroid Association (ETA) qui a permis la mise en œuvre d’un consensus pour la prise en charge du cancer différencié de la thyroïde (CDT). Les experts désignés pour chaque pays ont pu identifier les problèmes diagnostiques et thérapeutiques les plus significatifs, ce qui a permis l’élaboration de cet accord.
L’hormonothérapie avant 2015
Avant 2015, les spécialistes prévenaient la stimulation des cellules thyroïdiennes possiblement cancéreuses en s’assurant que la thyréostimuline, TSH, soit maintenue aussi basse que possible (entre 0,1 et 0,001). Ceci nécessitait une administration à vie, pour tous les patients, de fortes doses de lévothyroxine, une hormone thyroïdienne de synthèse.
Les études les plus récentes ont pu montrer que les effets indésirables de ce traitement – principalement les problèmes cardiaques et l’ostéoporose – étaient plus importants que les risques de récidive chez les sujets présentant des cancers dont les pronostics étaient bons.
Nouvelles recommandations d’hormonothérapie
Les nouvelles recommandations pour le traitement du cancer de la thyroïde ont permis de définir plusieurs catégories de risques. Le traitement est ainsi affiné, personnalisé en fonction de chaque cas et offre un meilleur suivi des risques de récidive.
Pour les personnes opérées d’un cancer thyroïdien, la dose de lévothyroxine qui est aujourd’hui recommandée est de l’ordre de :
- 2 à 2,5 μg/kg/j en traitement frénateur,
- et de 1,6 à 2 μg/kg/j en traitement substitutif.
Le dosage doit être proportionnel au poids et une connaissance préalable des facteurs susceptibles de majorer ou de minorer les besoins hormonaux permettra de prescrire le traitement le plus adéquat.
Quant aux risques cardiaques et osseux, leur prévention chez les sujets âgés ou chez les personnes contraintes de suivre un traitement puissamment frénateur s’effectue grâce à l’utilisation de bêtabloqueurs, de diphosphonates. En outre, un suivi régulier de l’état cardiaque chez les personnes fragiles ou âgées et de l’état osseux chez les femmes ayant dépassé l’âge de la ménopause est particulièrement recommandé.
La chirurgie de la thyroïde avant les nouvelles recommandations
Avant 2015, la thyroïdectomie totale était considérée comme le traitement de choix pour soigner le cancer de la thyroïde. Le but de cette intervention était de prévenir et de diminuer les risques de récidive et de morbidité, de faciliter le traitement post-opératoire par l’iode radioactif et d’améliorer la surveillance postopératoire.
Un curage ganglionnaire était parfois pratiqué, selon les cas : une exérèse ganglionnaire avait lieu systématiquement en cas de ganglion cancéreux palpable ou visible à l’échographie, et un curage prophylactique était réalisé en traitement de prévention.
Celui-ci permettait de retirer des ganglions potentiellement cancéreux après un examen anatomopathologique au microscope ou si le cancer avait été découvert inopinément au cours d’une première chirurgie réalisée pour des nodules bénins.
Aujourd’hui, une chirurgie différenciée…
Avec les nouvelles directives en matière de chirurgie de la thyroïde, la thyroïdectomie totale n’est pas appliquée au cancer bien différencié de la thyroïde, unifocal, avec un diamètre inférieur à 1 centimètre et sans métastases ganglionnaires, ni antécédents d’irradiation cervicale.
Pour ce type de cancers, une exérèse de la moitié de la thyroïde seulement peut être pratiquée (lobectomie seule). Quant au curage ganglionnaire, ce dernier est moins fréquent puisqu’il n’a lieu qu’à des fins préventives, si un ganglion cancéreux est visible à l’échographie, en latéral. Dans ce cas précis, un curage ganglionnaire central est alors pratiqué.
En outre, afin de minimiser les complications postopératoires, de plus en plus de chirurgiens s’appuient sur l’efficacité du dispositif d’imagerie par autofluorescence, FLUOBEAM® LX, qui permet d’identifier avec une haute précision les glandes parathyroïdes (qui se trouvent à proximité de la thyroïde) afin de les préserver. Du côté des patients, cette technologie constitue une grande avancée dans le traitement chirurgical de la thyroïde car elle permet, selon certaines études, de diminuer le taux d’auto-transplantation et de réduire l’hypoparathyroïdie postopératoire.
L’iode 131
En médecine, l’iode-131 est utilisé sous forme de gélules dans le cadre de la scintigraphie thyroïdienne qui étudie le fonctionnement de la glande thyroïde. En outre, il est parfois utilisé en traitement de l’hyperthyroïdie chez les patients qui nécessitent des soins rapides. Il permet également de contrôler l’hyperthyroïdie avant que la thyroïde ne soit retirée.
Pour les patients atteints de cancer de la thyroïde, le recours à l’iode 131 offre une meilleure surveillance de la maladie et prévient les risques de récidive après la chirurgie.
Avant 2015, l’iode 131 était communément utilisé comme traitement complémentaire des cancers de la thyroïde, sous forme de gélule orale avec un dosage qui variait entre 20 et 50 mCl, selon les centres en France.
La radiothérapie par iode 131, ou irathérapie, était principalement pratiquée en traitement adjuvant dans le but de rechercher d’éventuels foyers tumoraux et d’assurer leur destruction
Ceci permettait également de faciliter la surveillance de la maladie, de surveiller son évolution et d’obtenir une thyroglobuline basse. L’efficacité de cette technique n’est toutefois avérée que sur des cancers iodo-sensibles qui représentent moins de 30 % des cas.
C’est pourquoi aujourd’hui, l’intérêt de l’iode 131 est remis en question. Car, bien qu’il puisse détruire les cellules thyroïdiennes normales et cancéreuses, la surveillance s’avère déjà facilitée dans certains cas et son avantage sur la survie des patients est controversé.
Bon à savoir :
Les tumeurs thyroïdiennes sont généralement bénignes. Quant aux tumeurs malignes, elles représentent moins de 1 % des cas diagnostiqués chaque année.
Ne manquez pas notre article Cancer low risk : surveillance pour le cancer de la thyroïde
Les avancées scientifiques et technologiques, à l’instar du dispositif d’imagerie FLUOBEAM® LX, ont rendu la prise en charge du cancer de la thyroïde moins lourde de conséquences, plus sécurisée et plus confortable pour les patients. Par ailleurs, les dernières recommandations concernant cette pathologie offrent aujourd’hui aux patients des traitements adaptés à leurs besoins, ce qui n’était pas possible jusqu’à très récemment. En outre, le suivi des cancers à faibles risques est aujourd’hui facilité par la pratique d’une échographie cervicale et d’un dosage de thyroglobuline.
Aussi, il convient de noter que dans la majorité des cas, une détection précoce du cancer de la thyroïde augmente les chances de guérison. Il est donc particulièrement recommandé de participer aux programmes de dépistage nationaux.